El primer teléfono de Alexander Graham Bell fue un éxito porque Bell fue capaz de generar sonido de la luz. Eso fue en 1880. Ahora, los investigadores de la Universidad de Arkansas para las Ciencias Médicas en Little Rock están usando el mismo principio para crear una novedosa herramienta de diagnóstico altamente sensitiva que tal vez pueda detectar cáncer y otras enfermedades antes de que se vuelvan mortíferas.
El nuevo “teléfono” de los investigadores combina un láser y un transductor de ultrasonido, que les permite escuchar células normales y anormales que fluyen a través del sistema linfático, una red complicada de vasos, ganglios, y órganos linfáticos. Además de sus otras funciones, este segundo sistema circulatorio trabaja directamente con el sistema circulatorio primario del cuerpo para transportar los desperdicios y nutrientes celulares a través del cuerpo. A pesar de que los investigadores saben que el sistema linfático juega un papel en el cáncer, en la inflamación, y en la lucha contra infecciones, poco se conoce acerca de la composición celular de la linfa y de cómo se mueven las células a través de esta red.
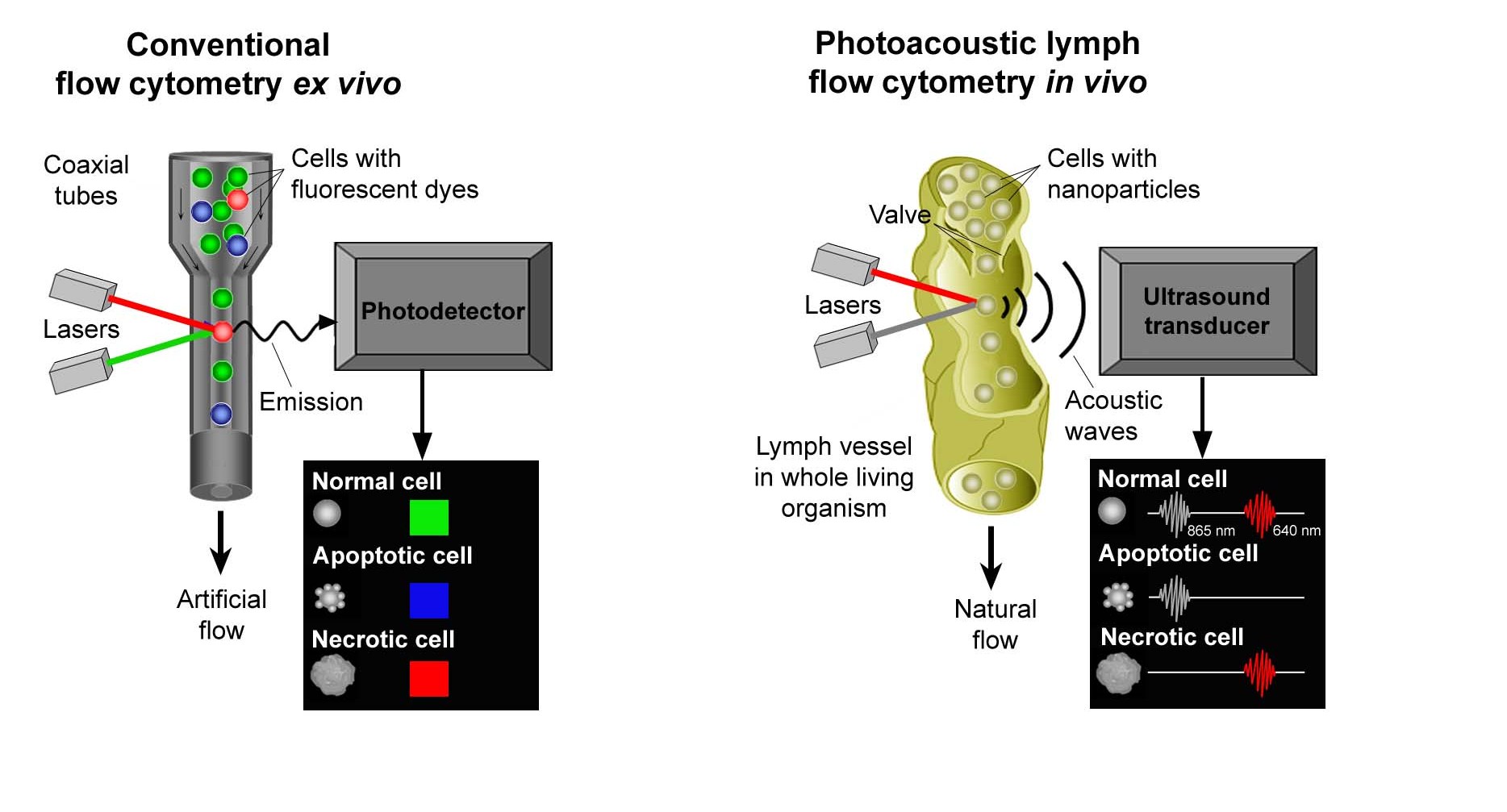
Esta novedosa técnica, citometría de flujo fotoacústico en vivo, fue desarrollada por Vladimir Zharov, director de los Laboratorios Philips de Láser Clásico y Nanomedicina en el Instituto de Cáncer Winthrop P. Rockefeller y profesor de otolaringología y radiología en la Universidad de Arkansas para las Ciencias Médicas, y su colega Ekaterina Galanzha. La técnica permitirá a los investigadores identificar y contar una amplia variedad de tipos de células, incluyendo aquellas relacionadas con infección, cáncer, y el sistema inmunológico del cuerpo. La investigación está basada en experimentos previos de Zharov y Galanzha con pruebas de sangre en vivo en las cuales pudieron encontrar un grupo de células de cáncer de piel entre mil millones de células.
Encontrar el Canal Linfático
Al comienzo del proyecto de la linfa, Zharov y Galanzha sabían que la linfa sería una sustancia difícil de trabajar. A diferencia del flujo de sangre, la linfa incolora tiene un flujo de doble sentido más lento e inestable. Los métodos actuales para tomar muestras de linfa capturan sólo unos cuantos microlitros de la sustancia pegajosa, haciendo que la toma de muestras de linfa sea impráctica para la prueba de enfermedades. “Reunir linfa de un sitio es un arte”, dice Zharov, pero “hay una cantidad enorme de información en el sistema linfático”.
Una técnica común de laboratorio, la citometría de flujo, cuenta e identifica células individuales mientras pasa una-por-una a través de un rayo de luz. Esta técnica invasiva remueve células de su ambiente nativo en pequeñas cantidades y tal vez altere las propiedades celulares. Convertir el arte en ciencia obligó a los investigadores a encontrar una manera no invasiva de manipular células linfáticas dentro de su ambiente nativo para que pudieran se contadas y examinadas.
El método de Zharov y Galanzha para resolver este problema es utilizar la red de control de tráfico del sistema linfático creado por la Madre Naturaleza. Una serie de pequeños tubitos llamados vasos linfáticos prenodales yacen justo por debajo de la superficie de la piel y se extienden a casi todos los tejidos del cuerpo. Unas válvulas en estos tubos mantienen el flujo celular en un sentido dentro del sistema linfático.
“Las células se mueven como un flujo multi-filas a diferentes velocidades y pueden cambiar frecuentemente de dirección, lo que puede hacer muy complicada su evaluación”, dice Zharov, pionero del uso de rayos láser para generar sonido para aplicaciones médicas a principios de los 1980s. “Aprendimos que las válvulas linfáticas pueden funcionar como boquillas que canalizan periódicamente cada célula en una línea recta". Al coordinar este fenómeno natural con pulsos láser individuales, Zharov y Galanzha pueden contar e identificar células individuales que fluyen en su ambiente natural. Este método permite un monitoreo a largo plazo de un mayor volumen de flujo linfático comparado con la toma de muestra en una sola vez de una cantidad pequeña de linfa.
Escuchar la Linfa
Para examinar las células linfáticas, Zharov y Galanzha aplican primero un nivel seguro de energía láser en la piel. La luz penetra de unos cuantos milímetros a unos cuantos centímetros a los vasos linfáticos llenos de células linfáticas fluyentes. Al escoger cuidadosamente el ancho de banda correcto, el rayo de luz calienta sólo las células que contienen biomoléculas que absorben luz llamadas cromóforos, tales como la hemoglobina y la melanina. La rápida expansión de cromóforos calientes ocasiona un cambio en la presión local. Esta acción crea un tipo particular de onda sonora, una onda fotoacústica, la cual viaja a través del tejido y es capturada por un transductor de ultrasonido en la superficie de la piel. Las ondas fotoacústicas viajan a velocidades específicas, haciéndolas más fáciles de detectar que las ondas genéricas provenientes de tejido adyacente.
En sus experimentos, Zharov y Galanzha encontraron que las células con alta pigmentación, tales como los glóbulos rojos y las células de melanoma (cáncer de piel), producían las ondas sonoras más fuertes y eran fácilmente localizadas sin agentes de imágenes adicionales. Para encontrar células no pigmentadas, tales como diferentes tipos de glóbulos blancos, los investigadores aplicaron nanopartículas de oro de diferentes colores para identificar glóbulos blancos en el flujo de la linfa y crearon ondas sonoras dobles utilizando dos pulsos láser en diferentes anchos de banda. Debido a que cada glóbulo blanco tiene un color característico individual, este método identificó células de flujo rápido cuyas características correspondían con las etiquetas de oro.
En un estudio animal preliminar para detectar melanoma metastásico (células de cáncer de piel que se han esparcido más allá del sitio original del tumor), la técnica fue tan sensitiva que detectó un grupo individual de células de melanoma entre un millón de glóbulos blancos en la linfa. Este prometedor resultado podría significar un incremento en la tasa de supervivencia al cáncer en humanos porque 90% de todas las muertes de cáncer resultan por metástasis. “La detección temprana de tumores antes de que se colonicen en metástasis detectable podría prevenir la metástasis o, al menos, reducir su velocidad de crecimiento, y podría ofrecer la oportunidad de eliminar células de tumor de la linfa y del flujo de sangre con terapias de láser convencionales o nuevas”, dice Galanzha.
Sonidos del Futuro
En un futuro, la técnica podría usarse muy dentro del cuerpo para evaluar linfa profunda y vasos sanguíneos en órganos con riesgo de enfermedad. Los investigadores de Arkansas están explorando ambos métodos no invasivo y muy poco invasivo para la detección temprana de infarto, ataque cardíaco, infecciones, e inflamación. El reto es compaginar las etiquetas de imagen correctas, o nanopartículas, con células objetivo de manera que se escuche claramente a las células anormales dentro del ambiente celular ruidoso.
A pesar de que experimentos recientes se han enfocado en estudios preclínicos con animales, el equipo planea enfocarse en ensayos clínicos en humanos en el próximo año o dos. Primero evaluarán las células en el flujo sanguíneo y después se enfocarán a evaluar la linfa. Zharov estima que evaluar el volumen completo de sangre de un adulto, como 5 litros de fluido, tomará como una hora. Futuros refinamientos deberán reducir ese tiempo como a 5-10 minutos. Las evaluaciones de linfa ocurrirán en extremidades como la pierna, donde los vasos linfáticos se localizan relativamente cerca de la piel.
Cuando la técnica esté clínicamente disponible, Zharov espera poder ofrecer un sistema combinado de diagnóstico/terapia. “Debemos ser capaces de matar células metastásicas en diseminación con el mismo láser que detecta las células anormales al incrementar la energía por un poquito”, dice él. Otras aplicaciones pueden incluir limpiar los fluidos corporales de bacteria y de otros virus y observar la reacción celular a la terapia de medicamentos y a la radicación.
“La evaluación de la linfa podrá ofrecer una forma completamente nueva de diagnóstico médico”, dice Zharov. “No será tan universal como una prueba de sangre, pero para algunas [aplicaciones] será más específica”.
Este trabajo fue apoyado en parte por el Instituto Nacional de Bioingeniería e Imágenes Biomédicas.
Referencias
Galanzha EI, Shashkov EV, Tuchin VV, Zharov VP. In vivo multispectral, multiparameter, photoacoustic lymph flow cytometry with natural cell focusing, label-free detection and multicolor nanoparticle probes. Cytometry A. 2008 Oct;73(10):884–94.
Olszewski WL, Tárnok A. Photoacoustic listening of cells in lymphatics: research art or novel clinical noninvasive lymph test. Cytometry A. 2008 Dec;73A(12):1111–3.
Zharov V, Galanzha E, Shashkov E, Khlebtsov N, Tuchin V. In vivo photoacoustic flow cytometry for monitoring of circulating single cancer cells and contrast agents, Opt Lett. 2006 Dec 15;31:3623–5.
Zharov VP, Galanzha EI, Shashkov EV, Kim J-W, Khlebtsov NG, Tuchin VV. Photoacoustic flow cytometry: principle and application for real-time detection of circulating single nanoparticles, pathogens, and contrast dyes in vivo. J Biomed Opt. 2007 Sep-Oct;12:051503.
Zharov VP, Galanzha EI, Tuchin VV. In vivo photothermal flow cytometry: imaging and detection of individual cells in blood and lymph flow. J Cell Biochem. 2006 Apr 1;97:916–32. Review.
Zharov VP, Letokhov VS. Laser Optoacoustic Spectroscopy. Springer-Verlag. Berlin, Heidelberg, New York. 1986.
